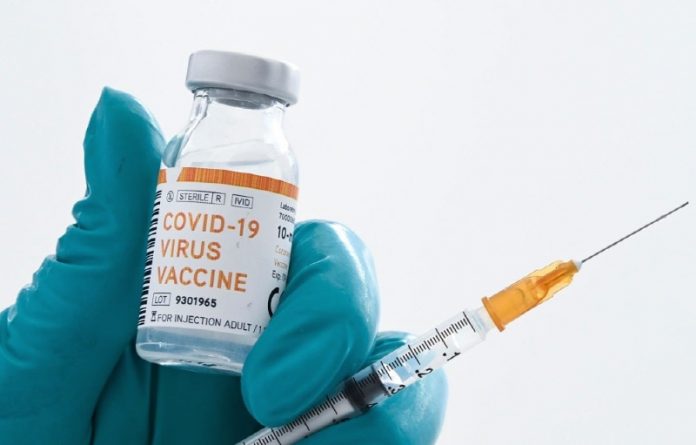
존슨앤존슨이 얀센 제약회사가 개발 증인 코로나19 백신 후보인 JNJ-78436735를 다국적으로 실험하는 ENSEMBLE프로젝트를 최근 시작했다. ENSEMBLE 실험 개시는 이 회사의 1/2a 단계 임상 연구로 얻은 긍정적인 중간과정 결과에 따른 것으로 한 번의 예방접종 후의 안전성과 면역 유전성이 추가 개발을 뒷받침한다는 것을 의미한다.
ENSEMBLE은 이 결과를 바탕으로 미국 식품의약국(FDA)와의 논의를 거쳐 3개 대륙에서 최대 6만 명의 자원봉사자를 등록해 코로나19 예방에 단일 백신 투여량 대 위약의 안전성과 효능을 연구하기 시작했다.
제조능력을 확대하며 매년 10억 회분의 백신을 제공하려는 목표 달성을 위해 노력중인 존슨앤존슨은 이 백신이 안전하고 효과적인 것이라고 입증될 경우 2021년 초부터 백신을 긴급 사용하도록 허가 작업을 추진 중인 것으로 알려졌다.
이에 따라 임상연구 프로토콜을 비롯해 3상 ENSEMBLE 연구와 관련된 정보를 투명하게 공유하려는 노력을 하고 있는 존슨앤존슨은 글로벌 전문가들로 구성된 연구 팀을 통해 내년 초 긴급 사용 허가를 위한 납품을 목표로 백신의 개발과 생산능력 확대에 박차를 가하고 있다.
얀센의 코로나19 백신 후보는 자사의 AdVac® 기술 플랫폼을 활용해 그동안 10만명 이상의 환자들에게 백신을 접종해왔다. 얀센 유럽 위원회가 승인한 에볼라 백신을 개발 및 제조하고 지카 바이러스, RSV, HIV 백신 후보를 구성하는 데도 사용되었던 이 기술이 성공할 경우 -20°C에서 2년, 2~8°C에서 최소 3개월 동안 안정적인 약효를 유지할 것으로 보인다. 기존의 표준 백신 유통 경로와 호환되는 것을 목표로 개발 중인 이 백신은 유통 과정에서의 별도 인프라를 필요로 하지 않는 것을 목표로 한다.

3상 ENSEMBLE연구는 만 18세 이상 성인 6만 명까지 단일 백신 투여량 대 위약의 안전성과 효능을 평가하기 위해 고안된 무작위 이중 위약 제어 임상 시험으로 특히 만 60세 이상의 성인을 대상으로 한다. 코로나 19의 진행 위험 증가와 관련해 합병증이 있는 사람과 없는 사람 모두를 포함하는 이 실험은 미국을 비롯해 아르헨티나, 브라질, 칠레, 콜롬비아, 멕시코, 페루, 남아프리카 등 확진 발생률이 높으면서도 신속한 착수 능력을 보유한 국가를 중심으로 진행된다.
ENSEMBLE은 기타거래약정 HHSO100201700018C에 따른 미국 보건복지부(HHS)의 준비 및 대응 담당 차관보실 산하의 바이오의학 첨단연구개발청(BARDA)를 비롯해 HHS에 있는 국립보건원(NIH) 산하의 미국 국립 알레르기 전염병 연구소(National Institute of Allergy and Infectious Diseases, NIAID)와의 협력으로 진행되고 있다. 존슨앤존슨은 영국 및 북아일랜드와 얀센 백신 후보의 2회 복용법을 연구하기 위해 여러 국가에서 별도로 3상 임상 시험에 관해 협력하기로 합의했다.
이 회사는 다른 한 편으로 백신이 안전하고 효과적이며 규제 승인을 따른다는 전제하에 이 제품이 전 세계에 사용될 수 있도록 여러 나라의 중앙 정부 및 글로벌 조직 등 많은 이해 당사자들과의 판매 시나리오도 준비중인 것으로 알려졌다.